海院科研动态(58)| 海洋天然产物4,4偶联氧杂蒽酮类二聚体Phomoxanthone A的生物合成途径及其二聚化功能研究取得最新进展
二聚化的天然产物广泛存在于真菌、细菌和植物中,通常具有比单体化合物更强的生物活性。其中,由丝状真菌所所产生的4,4偶联氧杂蒽酮类二聚体(Phomoxanthone A,PXA)具有更为显著的细胞毒活性和抗菌活性。目前,已有文献显示氧杂蒽酮类二聚体,如neosartorin、cladofulvin、secalonic acid D和cryptosporioptides等在进行2,4 或2,2偶联时,均需要邻位羟基进行导向,而在4位连接处没有邻位羟基的PXA的生物合成途径及其二聚化机制则未见报道。
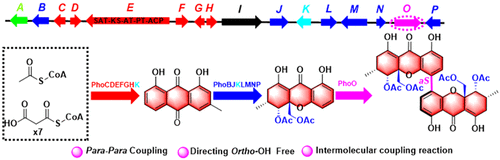
图1 PXA的生物合成基因簇及其生物合成途径
我院刘岚教授研究团队利用培养基优化、生物信息学分析、RT−qPCR分析和Crispr\Cas9基因敲除等方法,在一株海洋真菌Diaporthe sp. SYSU-MS4722中确定了PXA的生物合成基因簇(图1),并利用米曲霉Aspergillus oryzae NSAR1作为异源表达宿主对PXA的生物合成进行了解析。在该异源表达宿主中逐步表达14个基因,发现非还原性聚酮合酶(PhoE)和后修饰酶PhoCDFGHK主要负责聚酮骨架的构建和催化大黄酚(chrysophanol)的生成。转染基因phoBJKLMNP后发现,在Aspergillus oryzae中可以获得单体氧杂蒽酮penexanthone B,表明后修饰酶PhoBJKLMNP是催化大黄酚产生penexanthone B的重要合成途径(图1)。
随后,将二聚化酶(PhoO)导入产生单体penexanthone B的菌株中,最终获得二聚体PXA(图1)。进一步的喂养实验和体外微粒体实验结果表明,PhoO可通过催化penexanthone B区域选择性(para-para)的二聚化过程从而生成PXA。
与已报道的催化2,2-或2,4偶联的氧杂蒽酮二聚化酶不同,本研究所报道的PhoO是无需邻位羟基导向的、具有4,4偶联选择性的二聚化酶。该结果对研究结构多样性的蒽酮类二聚体合成具有重要的指导意义。
上述成果发表于中科院大类一区Top期刊《Organic Letters》(Yuan SiWen#, Chen SenHua#, Guo Heng, Chen LiTong, Shen HongJie, Liu Lan*, Gao ZhiZeng*, (2022) Elucidation of the Complete Biosynthetic Pathway of Phomoxanthone A and Identification of a Para-Para Selective Phenol Coupling Dimerase)。我院博士研究生元思文和副研究员陈森华为论文共同第一作者,高志增副教授和刘岚教授为共同通讯作者。
该研究得到广东省重点领域研发计划(2020B1111030005),国家自然科学基金(U20A2001)以及南方海洋科学与工程广东省实验室(珠海)自主科研项目(SML2021SP319)等基金的联合资助。
原文链接:https://pubs.acs.org/doi/abs/10.1021/acs.orglett.2c01050



